病気と治療

千葉大学大学院医学研究院
脳神経外科学
千葉大学病院
脳神経外科

Intensity Modulated Radiation Therapy:IMRT
千葉県がんセンター脳神経外科
井内俊彦
γ-knifeをはじめとした定位的放射線治療では、円柱状の放射線を標的に集中させることで、標的への高線量照射を可能としていますが、集中した放射線は必ず球体に近い線量分布を形成するという問題点も抱えています。
3次元原体照射(3D-CRT)は、照射される放射線の形を腫瘍の形に合わせることで、正常脳の被曝を最低限に避けようとする方法です。見る方向によって変化する腫瘍の投影像に合わせて放射線の形も変化させながら照射します。この方法を用いると、不整形をした腫瘍の形に合わせた線量分布の作成が可能ですが、それでも、腫瘍に食い込んでいたり、腫瘍の中を貫く正常組織を避けて照射することは困難でした。
IMRTは、この3D-CRTをさらに進化させた照射法です。照射を行う際に、腫瘍の形に単純に合わせるのでなく、腫瘍の中で照射線量に強弱をつける方法です。IMRTでは、直線加速器に取り付けられたMLC(multi-leaf collimator)と呼ばれるタングステンの板の重なりを、コンピューター制御で動かし、放射線の出てくる窓の形や大きさを変えながら照射を行います。こうすることにより、蓄積された放射線の量を、場所によって自由に変更することができるのです(図1)。

一方、IMRTのもう一つの特徴として、同時に異なる線量分布を作成できるSimultaneous Integrated Boostという照射法をあげることができます。例えば、腫瘍本体に強く照射を行い、その周囲に柔らかく照射を行うといったことが自由にできるのです(図3)。この照射法は特に浸潤性腫瘍において有効と思われ、千葉県がんセンターでは2002年から神経膠腫の治療にIMRTを応用し、優れた治療効果を証明しています。

IMRTは、①不正形腫瘍に対する対応が可能、②Simultaneous Integrated Boost法が可能、③分割照射が可能、などの点で、従来の照射やガンマナイフに代表される定位照射に比較してより自由度の高い優れた照射法ということができ、千葉県がんセンターでは全国に先駆けて神経膠芽腫治療への応用を行って参りました。(IMRTの項を参照)
この IMRTは通常直線加速器を固定した状態でMLC(multi-leaf collimator)を動かしながら照射を行い、これを多門で重ねていく方法をとりますが、最近、直線加速器を回転させながら IMRTを行っていく方法が開発されました。
VMAT(Volumetric Modulated Arc Therapy:強度変調回転照射)と呼ばれるこの照射法では、MLCの移動に伴う照射windowの変形による照射強度の変調と同時に、直線加速器の回転速度の変化でも照射強度を変更できます。これにより照射自由度はさらに改善され、多門IMRTの場合に生じる低線量領域の不均一性が解消され、よりconformityの良い線量分配を作成することが可能となりました。
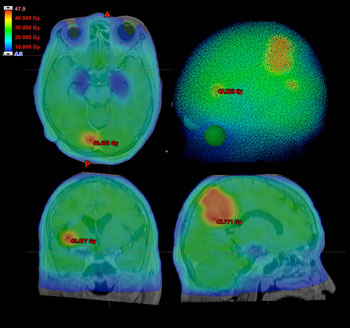
図1
多発転移性脳腫瘍例に対するVMAT 治療計画例(5分割照射)
MRIで確認できた3カ所の病変に対して辺縁線量40Gy(8Gy/Fr.)を照射しつつ、
全脳に20Gy(4Gy/Fr.)照射。海馬の被曝線量は10Gy未満に抑えられており、
眼球レンズは被曝していない。
VMATを用いると、例えば多発脳転移症例において、転移病巣に対して大線量照射を行いつつ全脳に低線量照射を同時に行い、かつ、海馬の被曝を避けると言った照射も可能となります(図1)。多発転移例におけるガンマナイフ治療は、異所性再発の危険性や、意図に反して正常脳に高線量被曝部位(hot-spot)が生じる危険性がある一方、従来の全脳照射では海馬の被曝に伴う学習記憶能力の低下の危険を伴っていました。VMATでは、脳全体に対する治療計画を作成するため、意図に反するhot-spotが生じる危険が少なく、また海馬の被曝を避けることで学習記憶能力低下を予防できると期待されています(海馬への転移発生の頻度は極めて低いことも報告されています)。この照射法では分割回数も自由に設定できるため、病変の大きさに対応した照射も可能です。さらに、従来のIMRTに比較して治療時間が短いのも特徴で、例えば図1の転移例に対する照射は1回数分で終了します。
悪性神経膠腫に対する照射においても、従来のIMRTに比較して照射時間の短縮により患者さんの負担は軽減し、また、一つの施設で治療できる患者数も増加しました。また、特に低線量領域の線量分布の改善により神経幹細胞の被曝線量を従来のIMRTよりも下げられることが分かっており、患者さんの長期的なQOL維持に寄与するものと期待されています。
千葉県がんセンターでは、確実なお病気の治療と機能温存の両立を目指して2011年にVMATを導入し、放射線治療部と連携して悪性脳腫瘍の治療に応用しています。